Benjamin Hampel1, 2, Cate Esson3, Bernard Surial4, Lukas Baumann4, Florian, Vock5, Jan Fehr 1 *
La prophylaxie pré-exposition contre le VIH (PrEP VIH) est une méthode permettant aux personnes exposées à un risque temporairement élevé de contracter le VIH de se protéger contre l’infection en prenant des médicaments antirétroviraux. Ces nouvelles recommandations ont été élaborées dans le cadre du programme SwissPrEPared, soutenu par l’Office fédéral de la santé publique (OFSP), et approuvées par la Commission fédérale pour les questions liées aux infections sexuellement transmissibles (CFIST) le 28 août 2025.
Ces recommandations ont été élaborées dans le cadre du programme SwissPrEPared afin d’aider les prestataires de santé à prescrire la PrEP VIH. Elles seront régulièrement adaptées, sur la base des connaissances scientifiques en constante évolution et de l’évaluation de la qualité du programme SwissPrEPared, et publiées sur le site : www.swissprepared.ch. Ces recommandations sont destinées à informer tous les personnels de santé qui prescrivent ou transmettent des informations sur la PrEP VIH. Les recommandations suivantes s’appuient sur les recommandations précédemment publiées par la Commission fédérale pour la santé sexuelle (CFSS)(1) et sur les résultats de l’étude SwissPrEPared et d’autres études et recommandations internationales(2)(3). Les prestataires de santé peuvent également rejoindre le programme national SwissPrEPared, et bénéficier d’une formation spécifique et d’autres formes de soutien. Lors de la publication de ces recommandations, la PrEP VIH ne peut être prise en charge, au titre de l’assurance obligatoire des soins, que pour les personnes qui reçoivent une prescription de PrEP VIH dans l’un des centres SwissPrEPared. Pour plus d’informations, veuillez contacter l’équipe de l’étude (www.swissprepared.ch).
Déclaration sur l’inclusion des genres
Les résultats concernant l’efficacité de la PrEP VIH orale diffèrent chez les hommes et les femmes cisgenres. Certaines populations, telles que les hommes et les femmes transgenres, restent encore peu représentées dans les études. Dans ces recommandations, nous avons inclus les connaissances actuelles, en tenant compte, autant que possible, de toutes les identités de genre. Nous avons toutefois conscience que nos recommandations n’incluent pas les personnes non binaires. Ce n’est pas parce que nous ne reconnaissons pas leur identité de genre. Nous avons la conviction que dépasser la conception binaire des genres constitue une avancée significative pour l’humanité toute entière. Cependant, comme peu d’études ont pris en compte les questions liées aux identités non binaires, et afin de rendre les recommandations les plus lisibles possibles, nous avons décidé d’éviter de mentionner spécifiquement les personnes non binaires dans le texte. Nous pensons actuellement que le fait d’inclure les personnes non binaires dans des groupes présentant un risque équivalent en raison de leur anatomie génitale et/ou de leur réseau sexuel, sans toujours les nommer, rend ces recommandations plus accessibles pour les personnes prescrivant la PrEP VIH. Par exemple, une personne non binaire qui a été assignée au sexe masculin à la naissance et qui a des rapports sexuels avec des hommes est très probablement mieux représentée dans le groupe épidémiologique des hommes cisgenres ayant des rapports sexuels avec des hommes (HSH cisgenres). Une personne non binaire assignée au sexe féminin à la naissance, présentant des caractéristiques sexuelles masculines et ayant des rapports sexuels avec d’autres HSH, est également mieux représentée dans le groupe HSH en raison du risque lié à son réseau sexuel. Comme il s’agit pour nous d’un processus continu, nous réévaluerons cette approche à chaque mise à jour de ces recommandations.
De vastes essais ont démontré la grande efficacité de l’association du ténofovir disoproxil (TDF) et de l’emtricitabine (FTC) utilisée en PrEP chez plusieurs groupes particulièrement exposés au VIH. L’efficacité s’est avérée la plus élevée chez les hommes cisgenres ayant des rapports sexuels avec des hommes (HSH). Les schémas thérapeutiques quotidiens et ponctuels ont tous deux montré une efficacité de 86 % dans la protection contre le VIH(4)(5) . L’efficacité chez les personnes qui présentent une bonne observance est encore plus élevée et estimée à environ 99 %(6) . Bien qu’une méta-analyse réalisée en 2015 n’ait révélé aucune différence dans l’efficacité du TDF/FTC entre les sexes, de nombreuses études ont montré une efficacité réduite chez les femmes cisgenres(7) . La plupart des études suggèrent que l’observance semble être un enjeu plus important pour les femmes cisgenres que pour les hommes cisgenres, et qu’un délai plus long est nécessaire pour l’initiation de la PrEP VIH avant d’atteindre des concentrations stables dans les tissus vaginaux(8)(9)(10). Cependant, en raison de la faible observance globale dans les essais cliniques randomisés (ECR) chez les femmes cisgenres, un seul ECR a démontré l’efficacité clinique chez les femmes cisgenres(11). En conséquence, les études de modélisation utilisant les données de ces ECR et émettant des hypothèses sur la nécessité d’une observance plus élevée chez les femmes cisgenres présentent des intervalles de confiance globalement larges et doivent donc être évaluées de manière critique. D’autres études et la réévaluation d’études pharmacocinétiques (EPC) antérieures contredisent ces résultats et suggèrent que l’observance et le délai d’initiation nécessaires sont les mêmes pour les femmes cisgenres que pour les hommes cisgenres(12)(8) . Bien qu’il n’existe pas encore d’études cliniques pour prouver cette nouvelle approche, de nouvelles molécules utilisables pour la PrEP VIH donnent des résultats prometteurs. Le cabotégravir et le lénacapavir injectables à longue durée d’action ont montré une meilleure efficacité que le TDF/FTC chez les femmes cisgenres, mais ne sont pour l’instant pas approuvés pour la prévention en Suisse(13)(14). De plus, leur coût élevé constitue un obstacle supplémentaire à leur utilisation hors autorisation de mise sur le marché (AMM). Il convient de noter que les deux essais ont montré que la faible observance de la PrEP VIH orale était à nouveau le principal facteur de réduction de l’efficacité chez les femmes cisgenres, et non un échec médical.
Il existe peu de données sur la PrEP VIH chez les hommes et les femmes transgenres(15). Par conséquent, pour ces deux groupes, le schéma de prise utilisé par les femmes cisgenres devrait être appliqué. La PrEP VIH s’est également révélée efficace contre l’infection chez les personnes qui prennent des substances psychoactives par injection et partagent leurs seringues, avec une réduction de 49 % de l’incidence du VIH(16). Cependant, dans cette étude, le ténofovir a été utilisé seul et non en association avec l’emtricitabine.
En Suisse, la PrEP VIH est recommandée depuis 2016 pour les personnes présentant un risque élevé d’infection par ce virus(1) . Depuis 2020, le TDF/FTC est approuvé par Swissmedic pour l’utilisation en PrEP VIH. Depuis le 1er juillet 2024, la PrEP VIH peut être prise en charge au titre de l’assurance obligatoire des soins si la prescription est faite par une personne participant au programme SwissPrEPared et conformément au document de référence de l’OFSP « Prophylaxie pré-exposition contre le VIH (PrEP VIH) » datant du 31 mars 2024(17) . Étant donné que les personnes qui utilisent la PrEP VIH sans suivi s’exposent potentiellement, elles-mêmes et autrui, à des risques sanitaires évitables, ces recommandations visent à garantir un suivi de qualité pour les personnes qui demandent la PrEP VIH, ainsi qu’à encourager les prestataires de santé à proposer un accompagnement aux personnes intéressées par la PrEP VIH.
3.1. Rôle des prestataires de santé dans le processus de prescription de la PrEP VIH
La décision finale concernant la prise de la PrEP VIH revient toujours à la personne concernée, sur la base d’une prise de décision partagée avec la personne prescriptrice. En 2015, l’OMS a recommandé la PrEP VIH pour les populations dont l’incidence annuelle du VIH était d’au moins 3 %(18) . Comme cette approche a conduit au refus de prescrire la PrEP VIH aux personnes exposées au VIH mais qui ne répondaient pas à ce seuil, la dernière mise à jour de l’OMS recommande que toutes les personnes qui demandent la PrEP VIH se voient accorder la priorité pour se voir proposer la PrEP VIH, car la demande elle-même peut indiquer un risque plus élevé de contracter le VIH(19). En Suisse, les efforts visant à atteindre les populations les plus exposées au VIH, principalement des hommes cisgenres et des personnes transgenres ayant des rapports sexuels avec des hommes, doivent se poursuivre, car nous ne constatons toujours pas de diminution suffisante du nombre de de ces groupes découvrant vivre avec le VIH(20) . D’autre part, pour atteindre les objectifs fixés pour 2030 en matière d’éradication de la transmission du VIH, des efforts supplémentaires sont nécessaires pour atteindre d’autres populations exposées au VIH qui pourraient également bénéficier de la PrEP VIH. Le risque individuel peut être contextuel : par exemple, des personnes qui ne sont pas considérées comme exposées au VIH en Suisse peuvent l’être d’avantage lorsqu’elles voyagent à l’étranger ; en outre, les comportements peuvent évoluer au fil du temps et les personnes qui à un moment ne tirent pas de bénéfice de la protection conférée par la PrEP VIH peuvent en bénéficier plus tard. La PrEP VIH n’est souvent nécessaire que pendant une certaine période de la vie. Cette période peut varier de quelques jours à plusieurs années d’une personne à l’autre. Le recours à la PrEP VIH comme protection contre le VIH est une décision individuelle et très personnelle. Les personnes qui demandent la PrEP VIH sont donc les mieux placées pour évaluer leur propre risque. En collaboration avec les prestataires de santé et à l’aide des informations fournies, elles peuvent établir la stratégie de protection optimale dans le cadre d’un processus décisionnel. Les prestaires de santé doivent être capables de faciliter ce processus décisionnel, de fournir des informations faciles à comprendre, d’exclure les contre-indications à la prise de la PrEP VIH et d’évaluer l’existence d’autres troubles de santé (tels que les troubles anxieux), car ceux-ci pourraient influencer le processus décisionnel et l’observance. Les personnes susceptibles de bénéficier de la PrEP VIH, celles qui n’en ont pas besoin et les contre-indications à la PrEP VIH sont répertoriées dans le tableau 1.
3.2. À qui recommander la PrEP VIH
Au-delà de l’importance de l’autodétermination dans le processus décisionnel pour ou contre la prise de la PrEP VIH, certaines personnes méritent une attention particulière car elles courent un risque plus élevé de contracter l’infection par le VIH et devraient donc être informées et se voir proposer la PrEP VIH lors de consultations. Les personnes qui peuvent le plus bénéficier de la protection conférée par la PrEP VIH sont répertoriées dans le tableau 1 :
Tableau 1 : à qui recommander la PrEP VIH et contre-indications du TDF/FTC utilisé pour la PrEP VIH
| Personnes susceptibles de bénéficier de la PrEP VIH | Personnes appartenant à des groupes à haute prévalence du VIH en Suisse :
|
ET qui présentent au moins l’un des critères suivants : | |
| |
| |
| |
| |
| |
Personnes issues de groupes à faible prévalence du VIH en Suisse :
| |
MAIS qui présentent au moins l’un des critères suivants : | |
| |
| |
| |
Personnes qui n’ont pas besoin de la PrEP VIH |
|
| |
| |
Contre-indications pour le TDF/FTC en tant que PrEP VIH |
|
| |
|
3.3. Personnes qui s’injectent des substances psychoactives
Grâce au succès des programmes de réduction des risques, la prise de substances psychoactives par voie intraveineuse ne constitue plus actuellement un risque majeur pour le VIH en Suisse(20). Nous recommandons donc de maintenir ces stratégies de réduction des risques bien établies et acceptées et de ne pas généraliser la PrEP VIH dans le cadre de ces programmes. La PrEP VIH peut être envisagée pour les groupes de personnes qui s’injectent des substances et qui ne sont pas encore touchés par ces programmes, notamment les personnes qui utilisent des substances par voie intraveineuse dans un contexte sexuel ou celles qui n’utilisent pas de matériel d’injection stérile.
3.4. PrEP VIH après une prophylaxie post-exposition contre le VIH (PEP VIH)
Les personnes, en particulier les hommes cisgenres ayant des rapports sexuels avec des hommes (HSH cisgenres), qui ont eu une indication pour une PEP VIH présentent l’un des risques les plus élevés de contracter le VIH(21) . Les informations sur la PrEP VIH doivent donc être transmises lors des consultations d’initiation et de suivi de la PEP VIH. Si la personne décide de commencer la PrEP VIH après la PEP VIH, l’approche pour démarrer la PrEP VIH peut être difficile et dépend du risque estimé d’exposition future au VIH. Dans certains cas, attendre les six semaines recommandées pour effectuer un dépistage VIH de 4ème génération après avoir terminé un traitement PEP VIH peut être trop long, car une nouvelle exposition au VIH peut avoir eu lieu pendant cette période. Dans ces cas, deux approches pratiques peuvent être envisagées.
Soit une PCR VIH peut être effectué avant de commencer la PrEP VIH après une période fenêtre plus courte, soit la PrEP VIH peut être commencée immédiatement après la fin de la PEP VIH. Si la PrEP VIH est commencée immédiatement après la fin de la PEP VIH, le moment de la séroconversion et donc le moment où toute recherche d’anticorps et/ou d’antigènes du VIH est fiable n’est pas clair. Il n’y a pas suffisamment de données pour déterminer si la PEP VIH conduit à un résultat PCR faussement négatif en cas d’infection par le VIH. Par conséquent, une PCR peut aider dans le processus de décision, mais n’exclut pas totalement une infection par le VIH avant le début de la PrEP VIH. Dans les deux situations – lorsque la fenêtre sérologique (window period) de six semaines n’était pas terminée avant le début de la PrEP VIH – les limites des dépistages doivent être discutées avec la personne concernée et des dépistages du VIH doivent être effectués régulièrement durant le suivi tant que la PrEP VIH est prise et lorsque celle-ci est interrompue. Le tableau 2 peut être utilisé pour aider à prendre ces décisions. Il est possible de contacter les médecins de SwissPrEPared pour discuter d’un cas individuel si nécessaire.
Tableau 2 : Considérations relatives au risque futur d’infection par le VIH chez les personnes à qui l’on prescrit une PEP VIH
Risque estimé pour les situations à risque futur d’infection par le VIH | Exemples pratiques | Approche clinique |
Faible | Les préservatifs sont toujours utilisés lors des rapports avec des partenaires en dehors d’une relation exclusive. La situation à risque est due à un problème technique (ex. le préservatif s’est rompu pendant le rapport sexuel). | Le début de la PrEP VIH peut être reporté jusqu’à la consultation finale standard 6 semaines après la fin de la PEP VIH, y compris un test VIH de 4ème génération.
|
Moyen | Les préservatifs ne sont pas toujours utilisés, par exemple en raison de stratégies de protection insuffisantes (par exemple, le « séro-triage »), mais la personne peut confirmer de manière crédible qu’elle n’aura aucun problème à utiliser des préservatifs pendant les six semaines suivant la fin de la PEP VIH. | En fonction du risque individuel, envisager de réaliser une PCR VIH 21* jours après la fin de la PEP VIH avant de commencer la PrEP VIH. |
Élevé | Utilisation irrégulière du préservatif, de multiples prescriptions de PEP VIH, utilisation sexualisée de substances (ex. Chemsex) ou problèmes de santé mentale conduisant à des situations à risque. | En fonction du risque individuel, envisager de commencer la PrEP VIH directement après la PEP VIH. Revoir la personne toutes les 4 semaines pour un dépistage du VIH pendant les 3 à 6 premiers mois. |
À ce jour, l’association de 245 mg de ténofovir disoproxil fumarate (TDF) et 200 mg d’emtricitabine (FTC) est le seul médicament approuvé pour la PrEP VIH en Suisse. Le chapitre suivant fait référence à des molécules qui ne peuvent pas être prescrites pour la PrEP VIH en Suisse ou qui ne peuvent être prescrites qu’en dehors des indications approuvées.
L’association ténofovir alafénamide 25 mg (TAF) et emtricitabine (FTC) a été étudiée chez les hommes cisgenres ayant des rapports sexuels avec des hommes (HSH cisgenres) et les femmes transgenres et a démontré sa non-infériorité lorsqu’elle est utilisée en prise quotidienne(22) . En 2019, elle a été approuvée aux États-Unis (US) pour la PrEP VIH chez les HSH, mais jusqu’à présent, elle ne l’est pas dans l’Union européenne et en Suisse. Cette association peut être envisagée en dehors des indications approuvées pour les personnes présentant un risque élevé d’infection par le VIH et un risque de développer des lésions rénales. Cependant, l’autorisation américaine pour TAF/FTC ne concerne officiellement que les personnes dont le débit de filtration glomérulaire estimé – DFGe (estimate Glomerular filtration rate – eGFR) est supérieur à 60 ml/min (www.fda.gov). Le prix élevé de ce produit en Suisse constitue un autre obstacle. Si une évaluation clinique conduit à estimer qu’une personne présentant une contre-indication au TDF/FTC pourrait bénéficier du TAF/FTC, nous recommandons de contacter un centre spécialisé dans la PrEP VIH.
L’Organisation mondiale de la santé (OMS) considère que la lamivudine et l’emtricitabine (FTC) sont interchangeables en association avec le ténofovir disoproxil fumarate (TDF) pour la prévention du VIH(19) . Cependant, en raison du manque de données sur la PrEP VIH intermittente, nous ne recommandons pas cette association tant que des données supplémentaires ne seront pas disponibles.
Le ténofovir disoproxil fumarate (TDF) seul n’a pas été étudié chez les hommes cisgenres ayant des rapports sexuels avec des hommes (HSH cisgenres) et n’est donc pas recommandé pour la prévention du VIH en Suisse.
Des injections intramusculaires toutes les huit semaines de l’inhibiteur d’intégrase cabotégravir se sont révélées supérieures à la prise quotidienne de TDF/FTC dans la prévention des infections par le VIH pour les hommes cisgenres ayant des rapports sexuels avec des hommes (HSH cisgenres) et les femmes transgenres(23) ainsi que pour les femmes cisgenres(13). Cependant, les données en vie réelle font actuellement défaut. Aux États-Unis, le cabotégravir est approuvé pour la prévention du VIH depuis décembre 2021. Il n’a pas encore été approuvé pour la PrEP VIH en Suisse. Une utilisation hors AMM (autorisation de mise sur le marché) est théoriquement possible, mais son coût élevé en fait une option peu viable.
Le lénacapavir est un nouvel inhibiteur de la capside du VIH. Par rapport au TDF/FTC et au TAF/FTC par voie orale, une injection sous-cutanée semestrielle de lénacapavir a montré une incidence significativement plus faible du VIH chez les femmes cisgenres, les hommes cisgenres ayant des rapports sexuels avec des hommes (HSH cisgenres) ainsi que chez les personnes trans et de genre divers (14)(24) . Le produit n’est actuellement pas disponible ni approuvé pour la prévention du VIH en Suisse.
Le DVR est un anneau en silicone contenant de la dapivirine, un inhibiteur non nucléosidique de la transcriptase inverse, administré par voie vaginale pendant 28 jours. Lors d’essais cliniques, le DVR a réduit le risque d’acquisition du VIH de 27 à 31 % sans poser de problèmes de sécurité ni augmenter le risque de résistance aux médicaments anti-VIH(25)(26) . Le DVR est disponible dans 11 pays africains, mais pas en Suisse.
Des études sur d’autres médicaments sont en cours et pourraient déboucher à l’avenir sur d’autres schémas thérapeutiques pour la PrEP VIH.
5.1. Début et arrêt (phase d’initiation/phase de sevrage)
Alors que les premiers essais cliniques utilisaient des phases d’initiation et d’arrêt de la PrEP VIH plus longues, de 7 à 28 jours avant et après une pénétration anale ou vaginale sans préservatif, de plus en plus de données viennent étayer l’intérêt de phases d’initiation et d’arrêt plus courtes. Pour les hommes cisgenres ayant des rapports sexuels avec des hommes (HSH cisgenres), une phase d’initiation et de sevrage plus courte est envisageable, comme le démontrent plusieurs études suivant le protocole IPERGAY, également appelé régime « à la demande », « intermittent », « discontinu », « 2-1-1 » ou « Dx2 » (5)(27) . L’étude IPERGAY a évalué la PrEP VIH avec l’association ténofovir disoproxil fumarate et emtricitabine (TDF/FTC) initiée par une double dose de 2 à 24 heures avant le rapport sexuel et close après le rapport par une dose 24 heures après la première (double) dose et une dernière dose 24 heures plus tard (posologie « 2-1-1 »). Pour les rapports sexuels consécutifs, les HSH cisgenres ont reçu pour instruction de continuer à prendre un comprimé par jour jusqu’à deux jours après le dernier rapport sexuel. Avant chaque nouveau rapport sexuel, la PrEP VIH devait être initiée avec une double dose, sauf si la dernière dose de PrEP VIH avait été prise dans les 7 jours précédents, auquel cas une seule dose était recommandée pour réinitiée la PrEP VIH.
Pour les femmes cisgenres et les autres personnes ayant des rapports sexuels vaginaux réceptifs (y compris les hommes transgenres), une phase d’introduction et de sevrage plus longue de 7 jours était auparavant recommandée, en raison d’études pharmacocinétiques montrant des niveaux plus faibles et une décroissance plus rapide du ténofovir dans les tissus vaginaux. Cependant, ces études montrent en réalité que des niveaux protecteurs de TDF/FTC combinés ont été atteints dans 98 % des cas 2 heures après la prise orale de 2 comprimés de TDF/FTC(8) . En ce qui concerne la phase d’arrêt optimale, la même étude montre que la concentration était de courte durée par rapport aux tissus colorectaux et qu’une phase d’arrêt de 7 jours devrait donc toujours être recommandée aux femmes cisgenres et aux autres personnes ayant des rapports sexuels vaginaux réceptifs. De nombreuses directives internationales incluent donc déjà le nouveau régime dit « 2-7 » ou « Dx7 » pour ces personnes. Bien qu’il n’existe à ce jour aucune donnée clinique sur ce régime, nous pensons néanmoins que les preuves sont suffisantes pour le recommander aux personnes qui, sans cela, pourraient ne mettre en œuvre aucune protection efficace contre le VIH. Il est toutefois important que les femmes cisgenres et les autres personnes ayant des rapports sexuels vaginaux réceptifs soient informées de ce niveau de preuve réduit lors de la consultation pour la PrEP VIH.
Bien que les connaissances sur le moment idéal pour initier et arrêter la PrEP VIH s’améliorent, certaines situations nécessitent des précautions particulières :
D’autres schémas thérapeutiques, tels que la PrEP VIH continue quatre jours par semaine (TTSS = mardi, jeudi, samedi et dimanche), se basent uniquement sur des données rétrospectives et ne sont donc pas recommandés tant que des preuves supplémentaires ne seront pas disponibles (études en cours).
Figure 1 : Phases d’introduction et d’arrêt de la PrEP VIH orale (TDF/FTC)

5.2. Durée de la prise de PrEP VIH
La fréquence d’expositions sexuelles potentielles au VIH variant d’un individu à l’autre, la durée de la prise de la PrEP VIH varie également. Outre la prise quotidienne continue, qui est le traitement le plus courant, certaines personnes ayant des rapports sexuels moins fréquents préfèrent un traitement ponctuel, dans lequel la PrEP VIH n’est prise qu’avant et après un rapport sexuel.
Un schéma intermédiaire de la « PrEP intermittente » est souvent appelée « PrEP de vacances », et consiste à prendre la PrEP VIH quotidiennement uniquement pendant des périodes limitées et avec de longs intervalles sans PrEP VIH.
Les personnes qui demandent la PrEP VIH seront évaluées lors d’une visite initiale (voir la description ci-dessous). Pour celles qui décident de commencer la PrEP VIH, une deuxième visite, dite visite de sécurité, est recommandée quatre semaines après le début de la PrEP VIH afin d’évaluer les effets indésirables précoces et d’exclure toute infection aiguë par le VIH qui n’aurait pas été détectée lors de la visite initiale (fenêtre sérologique du dépistage VIH). Après la deuxième visite, une visite de suivi tous les 3 mois est recommandée pour toutes les personnes utilisant la PrEP VIH en continu, une visite de suivi tous les 3 à 6 mois pour les personnes utilisant la PrEP VIH de manière discontinue, et une consultation tous les 6 à 12 mois pour les personnes exposées au VIH qui ont décidé de ne pas prendre la PrEP VIH.
Plusieurs études évaluent actuellement si un intervalle plus long entre les visites pourrait être suffisant et plus rentable. La fréquence des dépistages des IST fait l’objet de nombreuses discussions et de recherches en cours dans le cadre de l’étude SwissPrEPared. La cohorte australienne a démontré qu’un sous-groupe d’utilisateurs de PrEP VIH, à savoir 25 %, recevaient 76 % des diagnostics d’IST(30) . Alors que les études actuelles peinent à présenter des facteurs de risque prédictifs clairs et précis pour aider les prestataires de santé à déterminer quelles personnes utilisatrices de la PrEP présentent un risque élevé d’IST et lesquelles présentent un risque plus faible, les visites de suivi tous les 3 mois restent la norme pour les personnes qui utilisent la PrEP VIH en continu. Cependant, des visites de suivi tous les 6 mois semblent acceptables si la personne :
6.1. Recommandations générales pour chaque visite
Outre les analyses de laboratoire recommandées, chaque visite doit :
6.1.1. Détection des troubles de santé mentale et de l’usage de substances psychoactives
Combiner l’évaluation de la santé mentale avec les consultations PrEP VIH présente deux avantages. Premièrement, les personnes particulièrement exposées au VIH appartiennent souvent à des minorités sexuelles et de genre et/ou autre qui sont fréquemment exposées à la stigmatisation, à la discrimination et à la violence. Cela les expose à un risque plus élevé de dépression et d’autres difficultés de santé mentale ainsi qu’à l’usage de substances psychoactives. Deuxièmement, il a été démontré que les troubles de santé mentale, en particulier la dépression, et l’usage de substances, peuvent nuire à l’observance de la PrEP VIH. Nous recommandons donc d’évaluer la santé mentale des personnes à chaque visite pour la PrEP VIH, soit lors d’une conversation directe, soit à l’aide d’un outil de dépistage validé tel que le Patient Health Questionnaire-4 (PHQ-4), qui est inclus dans l’outil de consultation SwissPrEPared.
6.1.2. Conseils sur l’observance
L’observance du traitement est l’élément le plus critique de l’efficacité de la PrEP VIH. Nous recommandons donc d’évaluer l’observance de la PrEP VIH à chaque visite et de soutenir les personnes qui rencontrent des difficultés à respecter leur schéma de prise.
Plusieurs mesures ont démontré leur efficacité pour améliorer l’observance :
6.2. Visite initiale
Les points suivants doivent être abordés lors de la visite initiale :
En cas de contre-indication à la PrEP VIH, d’autres stratégies de protection contre le VIH doivent être envisagées. Si une personne prend déjà la PrEP VIH à la première consultation dans le service, les interventions seront adaptées en conséquence. Si une personne remplit les conditions requises pour bénéficier de la PrEP VIH mais refuse de la prendre, un suivi tous les 3 à 12 mois est recommandé afin de réaliser des dépistages du VIH et d’autres IST.
6.3. Visite de sécurité
Les éléments suivants doivent être réalisés 4 semaines après le début de la PrEP VIH :
6.4. Visites de suivi
Une visite de suivi est faite 3 mois après la visite de sécurité, puis tous les 3 mois. L’intervalle peut être prolongé jusqu’à 6 mois entre deux visites de suivi pour une utilisation discontinue de la PrEP VIH et/ou en fonction du risque individuel.
Les éléments suivants doivent être réalisés lors d’une visite de suivi :
Les examens suivants doivent être effectués tous les 12 mois :
Tableau 4 : Calendrier des rendez-vous et principales évaluations cliniques
Visite initiale | Visite de sécurité | Visite de suivi
(Tous les 3 mois la première année, puis tous les 3 à 6 mois selon le risque) | Tous les 12 mois | |
Conseils sur la PrEP VIH, comprenant :
| x | |||
Ré)évaluation de l’indication, du schéma de prise et de l’observance dans la prise de la PrEP VIH | x | x | x | |
Évaluation des effets indésirables, y compris les interactions avec les médicaments ou compléments alimentaires concomitants. | x | x | x | |
Évaluation des risques comportementaux | x | x | ||
Symptômes d’une infection aiguë par le VIH (< 1 mois) | x | x | ||
Adhérence au traitement et accompagnement psychologique | x | x | x | |
Satisfaction de la personne sur le conseil | x | x | x | |
Dépistage VIH de 4ème génération (labo) | x | x | x | |
Dépistages d’IST bactériennes (syphilis, gonorrhée, chlamydia) | x | x | ||
Sérologie pour l’hépatite C | x | x Plus fréquemment si un comportement à risque spécifique est signalé. Voir 6.4 | ||
Sérologies pour l’hépatite B | x | |||
Évaluation du statut vaccinal | x | |||
Taux de créatinine sérique | x | x | x | |
Rapport protéines/créatinine | x | |||
| ALT | x | x | x Plus souvent, si élevé. Voir 8.3. |
Des dépistages réguliers des IST bactériennes ont été initialement inclus dans les consultations pour la PrEP VIH, dans l’espoir de réduire le nombre d’IST bactériennes au fil du temps au niveau de cette population, sur la base de modélisations mathématiques(31). Bien que les données de l’étude SwissPrEPared suggèrent un certain succès de cette approche de dépistage et de traitement (Test & Treat), aucune autre étude n’a pu prouver ce concept dans la vie réelle(32) .
Différentes approches ont été étudiées afin de réduire le nombre d’IST bactériennes dans cette population. Un certain optimisme s’est manifesté lorsque des études rétrospectives ont suggéré une immunité croisée chez les personnes ayant fait le vaccin méningococcique à vésicules de membrane externe du sérogroupe B (Bexsero® ), avec une réduction de 40 % des infections à gonorrhée(33) . Cependant, un essai randomisé a montré une faible réduction des cas de gonorrhée de 22 %, qui n’a pas atteint le seuil de signification statistique(34) . Compte tenu de ces résultats non concluants, actuellement nous ne recommandons pas l’utilisation hors indication (off label) du Bexsero® pour prévenir la gonorrhée chez les personnes utilisant la PrEP VIH.
De nombreuses études ont montré l’effet protecteur d’une dose de 200 mg de doxycycline administrée en prophylaxie post-exposition jusqu’à 72 heures après une exposition sexuelle potentielle chez les hommes cisgenres ayant des rapports sexuels avec des hommes (HSH cisgenres) et les femmes transgenres(34)(35) . Si la réduction du risque était de 70 % ou plus pour la chlamydia et la syphilis dans toutes les études, aucun bénéfice clair n’a été observé dans la prévention de la gonorrhée. De nombreuses directives recommandent donc la Doxy-PEP pour les HSH cisgenres et les femmes transgenres ayant une exposition aux IST bactériennes(36) . À San Francisco, où la Doxy-PEP est encouragée depuis octobre 2022, on observe une diminution des diagnostics de chlamydia et de syphilis au niveau de la population(37) . Bien que le Doxy-PEP semble être la première intervention à avoir eu un effet sur la réduction du nombre d’infections à chlamydia et à syphilis depuis des décennies, l’impact de l’utilisation généralisée de la doxycycline sur le développement de la résistance aux antimicrobiens et le microbiome reste incertain(38)(39). Nous encourageons les prestaires de santé proposant la PrEP VIH à parler ouvertement de la Doxy-PEP durant les consultations et à aborder les risques inconnus, d’autant plus que la prescription de doxycycline à des fins préventives n’est actuellement pas hors indication (Off-label).
À la date de publication du présent document, le CFIST travaille à l’élaboration de recommandations pour la Suisse.
8.1. Syndrome de démarrage de la PrEP VIH
Le syndrome de démarrage de la PrEP VIH décrit divers symptômes gastro-intestinaux et non gastro-intestinaux qui peuvent survenir dans les premiers jours aux premières semaines suivant le début de la PrEP VIH. Ils ne sont généralement pas associés à des lésions des organes et sont spontanément résolutifs après quelques jours, jusqu’à un maximum de 8 semaines(40).
Les effets indésirables peuvent inclure des nausées, des flatulences, des douleurs abdominales, des vertiges et des maux de tête. Ces symptômes apparaissent rapidement, mais disparaissent généralement au cours du premier mois. Ils peuvent souvent être traités par un traitement symptomatique, comme des analgésiques ou des antiémétiques, si nécessaire.
8.2. Altérations de la fonction rénale dues au TDF et surveillance recommandée
Le ténofovir disoproxil fumarate (TDF) est connu pour induire une tubulopathie rénale proximale (PRT), également appelée syndrome de Fanconi, chez certaines personnes(41) . Il s’agit d’un effet indésirable très rare dans lequel les tubules rénaux proximaux n’absorbent pas certains électrolytes et acides aminés, ce qui entraîne une élimination par l’urine. La protéinurie, l’hypophosphatémie, l’hypokaliémie, l’hypo-uricémie, l’acidose rénale et la glycosurie, avec un taux de glucose sanguin normal, sont caractéristiques de la PRT, tout comme une éventuelle insuffisance rénale et une polyurie. Dans le cas du PRT, il est possible que malgré la présence d’une protéinurie et d’une hypophosphatémie, la clairance de la créatinine reste dans la fourchette normale. Le plus souvent, seules certaines de ces anomalies sont observées, et il n’est pas certain que les tests permettent de distinguer au mieux la toxicité rénale du TDF.
8.2.1. Fréquence des tests de la fonction rénale
Après avoir commencé à prendre du TDF pour la PrEP VIH, une diminution faible mais statistiquement significative de la clairance de la créatinine peut être observée par rapport à la valeur de référence et celle-ci disparaît après l’arrêt du TDF/FTC(42) . Il n’existe aucune donnée pour les personnes dont le DFGe / eGFR est inférieur à 60 ml/min. Il n’est donc pas recommandé de poursuivre le traitement par TDF/FTC si le DFGe / eGFR tombe en dessous de 60 ml/min/1,73 m2.
La réduction de la clairance de la créatinine lors de la prise de TDF/FTC seul est un effet indésirable rare et de nombreuses directives internationales recommandent désormais de vérifier la fonction rénale seulement une ou deux fois par an chez les personnes prenant la PrEP VIH en bonne santé et ne présentant aucun autre risque d’insuffisance rénale (43)(44) . Bien que des tests tous les 6 à 12 mois puissent être suffisants pour les personnes ne présentant pas de facteurs de risque, nous recommandons un contrôle systématique de la fonction rénale à chaque visite pour les personnes considérées comme présentant un risque plus élevé, par exemple les personnes :
8.2.2. Comment dépister les troubles de la fonction rénal
8.2.3. Approche progressive en cas de DFGe / eGFR réduit
En cas d’altération de la fonction rénale, nous recommandons une approche par étapes (fig. 3)
Si une diminution du DFGe / eGFR est confirmée, nous recommandons les examens complémentaires suivants :
Si les analyses de laboratoire confirment une tubulopathie rénale proximale (PRT), arrêter le TDF/FTC et tester à nouveau la fonction rénale après 4 semaines. Un passage pour la PrEP VIH de l’association TDF/FTC à l’association TAF/FTC peut être envisagé (29). Cependant, l’utilisation du TAF/FTC pour la PrEP VIH est actuellement hors indication (off label) en Suisse (Swissmedic), et il n’existe pas de versions génériques disponibles dans les pharmacies suisses. Officiellement, l’indication aux USA (FDA) est restreinte aux personnes dont le DFGe / eGFR est supérieur à 60 ml/min.
Si les résultats de laboratoire ne confirment pas la PRT, envisager tout de même d’arrêter la PrEP VIH, en particulier si le DFGe / eGFR est inférieur à 60 ml/min, et orienter la personne vers un néphrologue.
Figure 3 : Approche par étapes en cas d’altération de la fonction rénale

8.3. Augmentation des taux d’enzymes hépatiques
Le ténofovir disoproxil fumarate (TDF) peut entraîner une augmentation légère à modérée de l’alanine aminotransférase (ALAT) hépatique chez certaines personnes vivant avec le VIH(45) ou prenant la PrEP VIH(46). La pertinence clinique de ces résultats n’est pas claire, et la plupart des lignes directrices ne recommandent pas d’inclure des tests ALAT dans les visites de suivi de la PrEP VIH(43)(44). À notre connaissance, aucun cas de lésion hépatique grave induite par la PrEP VIH n’a été signalé. Comme une légère élévation des enzymes hépatiques est fréquente dans la population générale (prévalence estimée à plus de 10 % dans la plupart des cas)(47), l’élévation des enzymes hépatiques chez les personnes prenant la PrEP VIH est susceptible d’avoir d’autres origines que la toxicité hépatique induite par le TDF, par exemple une maladie hépatique alcoolique (MHA ou ALD – alcoholic liver disease) ou une stéatohépatite non alcoolique (NASH – nonalcoholic steatohepatitis). La toxicité hépatique due à l’usage de substances psychoactives et à l’hépatite virale pourrait être plus fréquente chez les personnes prenant la PrEP VIH que dans le reste de la population.
Les avantages (détection précoce de la maladie et toxicité potentielle des médicaments) et les risques (surdiagnostic, arrêt inutile de la PrEP VIH, complications liées aux examens complémentaires, coûts) du dépistage chez les personnes prenant la PrEP ne sont pas clairs, et les données permettant de formuler une recommandation font défaut. En outre, la limite supérieure de la normale (LSN) pour les transaminases est contestée. Des valeurs dans la fourchette normale n’excluent pas les maladies hépatiques(48) , et l’évaluation diagnostique ultérieure des transaminases légèrement élevées ne permet souvent pas de détecter des maladies hépatiques spécifiques(34). Étant donné que la PrEP VIH est prescrite à des personnes en bonne santé à titre préventif, nous recommandons de tester l’ALAT avant de commencer la PrEP VIH, lors de la visite de sécurité puis tous les 12 mois, jusqu’à ce que davantage de données sur la toxicité hépatique soient disponibles.
Si une élévation des enzymes hépatiques est observée, d’autres causes que la prise de PrEP VIH doivent être envisagées. Pour les personnes non aigues et asymptomatiques, nous proposons une approche par étapes détaillée dans l’algorithme ci-dessous (fig. 4), que nous avons élaboré en nous inspirant des lignes directrices de l’EACS(3) . Lorsqu’une élévation persistante ou significative de l’ALAT (>2 x LSN) est observée, une évaluation de base des pathologies hépatiques les plus courantes doit être effectuée. Dans le cadre de cette évaluation de base, il convient d’évaluer la toxicité due à d’autres médicaments et substances (par exemple, les stéroïdes anabolisants, la cocaïne, l’ecstasy), une maladie hépatique alcoolique (MHA ou ALD – alcoholic liver disease) ou une stéatohépatite non alcoolique (NASH – Nonalcoholic steatohepatitis), une hémochromatose, une hépatite virale et les symptômes indiquant des maladies systémiques impliquant le foie. Les personnes doivent être évaluées pour détecter une stéatose hépatique à l’aide d’une échographie et, le cas échéant, une évaluation du risque de fibrose doit être réalisée à l’aide d’un score établi (par exemple, Fib-4)(48) . Un score à faible risque permet une réévaluation périodique. Pour les résultats modérés, il convient de réaliser une élastographie transitoire et, pour les scores à haut risque, il est recommandé de consulter un service d’hépatologie(3)(48). Si elle est disponible, une élastographie transitoire peut être envisagée dans le cadre de l’évaluation de base, mais dans la plupart des lignes directrices, l’échographie est recommandée comme premier outil de dépistage de la maladie du foie gras non alcoolique (NAFLD – non-alcoholic fatty liver disease) (3)(48)(49) .
Si aucune cause ne peut être identifiée et que l’élévation des enzymes hépatiques persiste, il convient d’évaluer les causes rares (maladies hépatiques auto-immunes et métaboliques). En outre, l’arrêt de la PrEP VIH et l’orientation vers un service d’hépatologie doivent être envisagés. En cas d’élévation significative des enzymes hépatiques (≥ 5,0 x LSN), d’apparition aiguë et/ou de symptômes, l’algorithme proposé doit être utilisé avec prudence et une évaluation complète et rapide ainsi qu’une orientation vers un service d’hépatologie doivent être envisagées. Il est important de souligner que la stéatose hépatique peut avoir plusieurs origines. Si, malgré des interventions sur le mode de vie, l’élévation de l’ALAT progresse ou qu’une fibrose se développe, d’autres causes doivent être envisagées.
Figure 4 : Approche par étapes en cas d’élévation de l’ALAT
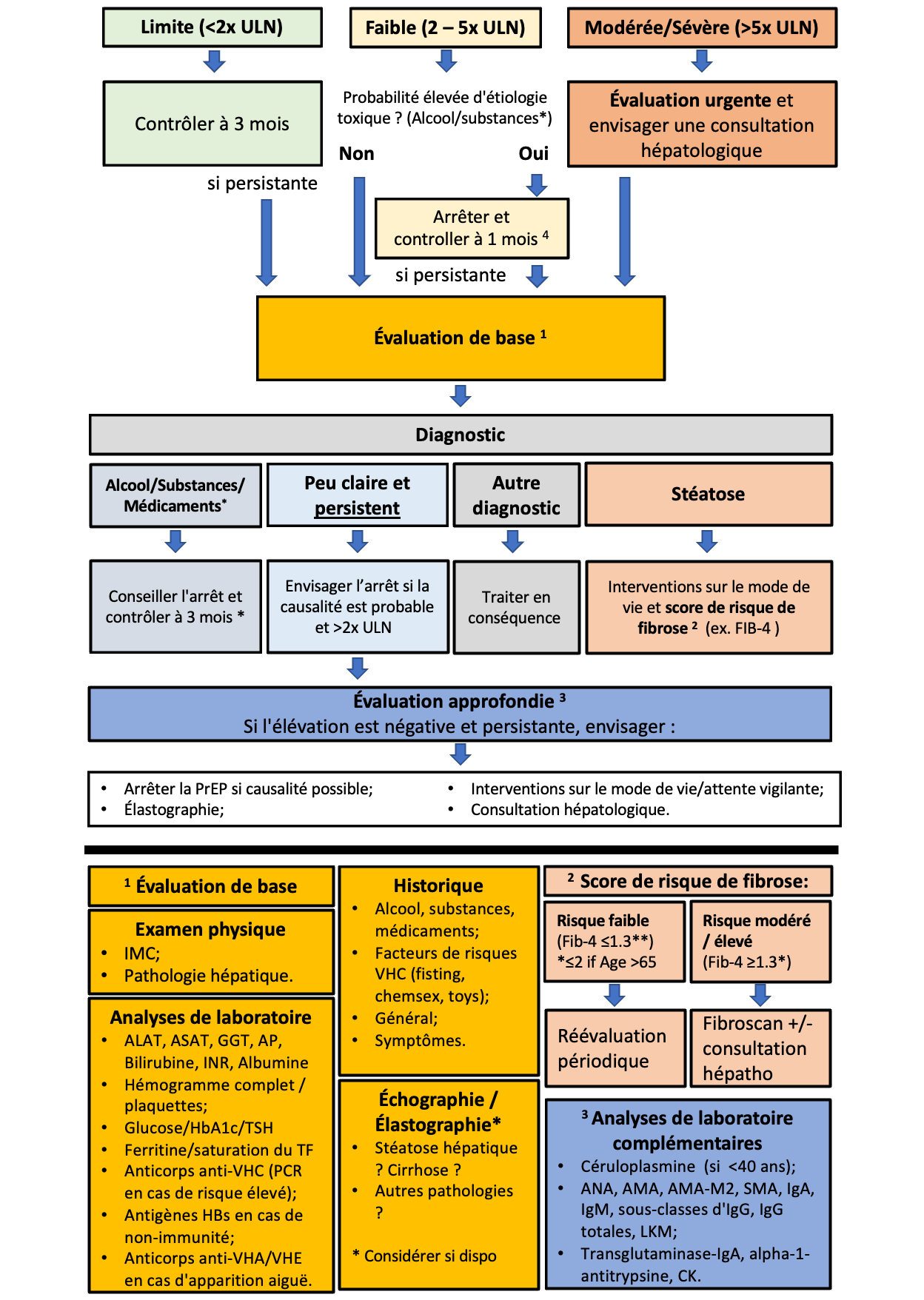
4 La consommation d’alcool et de substances entraînant une élévation des enzymes hépatiques est souvent causée par une consommation problématique ou une dépendance difficile à arrêter. Dans de telles situations, il est souvent insuffisant de conseiller d’arrêter et de refaire un test après un mois. Envisager une orientation vers un spécialiste en médecine des addictions
8.4. Diminution de la densité minérale osseuse (DMO)
La prise du ténofovir disoproxil fumarate (TDF) par les personnes vivant avec le VIH est associée à une diminution précoce de 3 à 4 % de la densité minérale osseuse après le début du traitement, en particulier lorsqu’il est co-administré avec un inhibiteur de protéase boosté(50). Pour les personnes ne vivant pas avec le VIH qui prennent le TDF/FTC comme PrEP VIH, cet effet semble moins prononcé (~1 %) sans augmentation du risque de fracture(42)(51)(51)(52). Aucun dépistage systématique par ostéodensitométrie n’est nécessaire pour les personnes prenant la PrEP VIH. Une activité physique accrue, l’arrêt du tabac et la réduction de la consommation d’alcool peuvent réduire le risque de fracture à long terme chez toutes les personnes, et une supplémentation en calcium peut être envisagée si l’apport est insuffisant. Le risque de fracture sur dix ans doit être évalué chez les personnes présentant des facteurs de risque d’ostéoporose (par exemple, antécédents de chutes ou de fractures, utilisation de glucocorticoïdes) à l’aide du score FRAX, et une ostéodensitométrie doit être réalisée chez les personnes présentant un risque élevé de fracture afin d’évaluer plus précisément la nécessité d’un traitement. Comme les conséquences cliniques de la diminution de la densité osseuse associée à la PrEP VIH restent incertaines, la décision de prescrire ou non une PrEP VIH à base de TDF/FTC en cas d’ostéoporose dépend du risque individuel d’infection par le VIH. Pour les personnes présentant moins de risques sexuels, le passage d’une prise continue à un schéma intermittent afin de réduire l’exposition au TDF pourrait permettre de réduire le risque d’une nouvelle diminution de la densité osseuse.
Bundesamt für Gesundheit. Empfehlungen der Eidgenössischen Kommission für sexuelle Gesundheit (EKSG) zur HIV-Prü-Expositionsprophylaxe (PrEP) in der Schweiz. BAG-Bulletin. 2016;(4).
Gandhi RT, Landovitz RJ, Sax PE, Smith DM, Springer SA, Günthard HF, et al. Antiretroviral Drugs for Treatment and Prevention of HIV in Adults: 2024 Recommendations of the International Antiviral Society–USA Panel. JAMA [Internet]. 2024 Dec 1 [cited 2025 Jan 29]; Available from: https://doi.org/10.1001/jama.2024.24543
Juan Ambrosioni, Jean-Michel Molina, Giovanni Guaraldi, Alan Winston, Christoph Boesecke, Paola Cinque, Alasadair Bamford Georg Behrens. EACS Guidelines 12.0. European AIDS Clinical Society. 2023;11.1.
McCormack S, Dunn DT, Desai M, Dolling DI, Gafos M, Gilson R, et al. Pre-exposure prophylaxis to prevent the acquisition of HIV-1 infection (PROUD): effectiveness results from the pilot phase of a pragmatic open-label randomised trial. Lancet (London, England) [Internet]. 2015/09/14 ed. 2016 Jan;387(10013):53–60. Available from: http://www.thelancet.com/pdfs/journals/lancet/PIIS0140-6736(15)00056-2.pdf
Molina JM, Capitant C, Spire B, Pialoux G, Cotte L, Charreau I, et al. On-Demand Preexposure Prophylaxis in Men at High Risk for HIV-1 Infection. The New England journal of medicine. 2015/12/02 ed. 2015 Dec;373(23):2237–46.
Anderson PL, Glidden DV, Liu A, Buchbinder S, Lama JR, Guanira JV, et al. Emtricitabine-tenofovir concentrations and pre-exposure prophylaxis efficacy in men who have sex with men. Science translational medicine. 2012/09/14 ed. 2012 Sep 12;4(151):151ra125.
Fonner VA, Dalglish SL, Kennedy CE, Baggaley R, O’Reilly KR, Koechlin FM, et al. Effectiveness and safety of oral HIV preexposure prophylaxis for all populations. Aids. 2016/05/06 ed. 2016 Jul 31;30(12):1973–83.
Cottrell ML, Yang KH, Prince HM, Sykes C, White N, Malone S, et al. A Translational Pharmacology Approach to Predicting Outcomes of Preexposure Prophylaxis Against HIV in Men and Women Using Tenofovir Disoproxil Fumarate With or Without Emtricitabine. The Journal of infectious diseases [Internet]. 2016/02/27 ed. 2016 Jul 1;214(1):55–64. Available from: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4907409/pdf/jiw077.pdf
Anderson PL, Marzinke MA, Glidden DV. Updating the Adherence–Response for Oral Emtricitabine/Tenofovir Disoproxil Fumarate for Human Immunodeficiency Virus Pre-Exposure Prophylaxis Among Cisgender Women. Clin Infect Dis [Internet]. 2023 Jan 16 [cited 2025 Feb 1];76(10):1850–3. Available from: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10209433/
Moore M, Stansfield S, Donnell DJ, Boily MC, Mitchell KM, Anderson PL, et al. Efficacy estimates of oral pre-exposure prophylaxis for HIV prevention in cisgender women with partial adherence. Nat Med [Internet]. 2023 Nov [cited 2025 Feb 1];29(11):2748–52. Available from: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC11386520/
Baeten JM, Donnell D, Ndase P, Mugo NR, Campbell JD, Wangisi J, et al. Antiretroviral Prophylaxis for HIV-1 Prevention among Heterosexual Men and Women. The New England journal of medicine [Internet]. 7AD Nov;367(5):399–410. Available from: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3770474/ https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3770474/pdf/nihms493581.pdf
Zhang L, Iannuzzi S, Chaturvedula A, Irungu E, Haberer JE, Hendrix CW, et al. Model-based predictions of protective HIV pre-exposure prophylaxis adherence levels in cisgender women. Nat Med [Internet]. 2023 [cited 2025 Feb 1];29(11):2753–62. Available from: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10667095/
Delany-Moretlwe S, Hughes JP, Bock P, Ouma SG, Hunidzarira P, Kalonji D, et al. Cabotegravir for the prevention of HIV-1 in women: results from HPTN 084, a phase 3, randomised clinical trial. Lancet. 2022/04/05 ed. 2022 May 7;399(10337):1779–89.
Bekker LG, Das M, Abdool Karim Q, Ahmed K, Batting J, Brumskine W, et al. Twice-Yearly Lenacapavir or Daily F/TAF for HIV Prevention in Cisgender Women. N Engl J Med. 2024 Oct 3;391(13):1179–92.
Sevelius JM, Deutsch MB, Grant R. The future of PrEP among transgender women: the critical role of gender affirmation in research and clinical practices. J Int AIDS Soc. 2016/10/21 ed. 2016;19(7(Suppl 6)):21105.
Choopanya K, Martin M, Suntharasamai P, Sangkum U, Mock PA, Leethochawalit M, et al. Antiretroviral prophylaxis for HIV infection in injecting drug users in Bangkok, Thailand (the Bangkok Tenofovir Study): a randomised, double-blind, placebo-controlled phase 3 trial. Lancet. 2013/06/19 ed. 2013 Jun 15;381(9883):2083–90.
Bundesamt für Gesundheit. Referenzdokument «HIV-Präexpositionsprophylaxe (HIV-PrEP). 2023.
WHO Guidelines Approved by the Guidelines Review Committee. In: Guideline on When to Start Antiretroviral Therapy and on Pre-Exposure Prophylaxis for HIV. Geneva: World Health Organization Copyright (c) World Health Organization 2015.; 2015.
Differentiated and simplified pre-exposure prophylaxis for HIV prevention: update to WHO implementation guidance [Internet]. [cited 2025 Jan 29]. Available from: https://www.who.int/publications/i/item/9789240053694
Bundesamt für Gesundheit. Sexuell übertragbare Infektionen und Hepatitis B/C in der Schweiz und Lichtenstein im Jahr 2023: eine epidemiologische Beurteilung. BAG-Bulletin 48. 2025 Nov 25;48/24:8–60.
Hovaguimian F, Günthard HF, Hauser C, Conen A, Bernasconi E, Calmy A, et al. Data linkage to evaluate the long-term risk of HIV infection in individuals seeking post-exposure prophylaxis. Nat Commun. 2021/02/24 ed. 2021 Feb 22;12(1):1219.
Mayer KH, Molina JM, Thompson MA, Anderson PL, Mounzer KC, De Wet JJ, et al. Emtricitabine and tenofovir alafenamide vs emtricitabine and tenofovir disoproxil fumarate for HIV pre-exposure prophylaxis (DISCOVER): primary results from a randomised, double-blind, multicentre, active-controlled, phase 3, non-inferiority trial. The Lancet [Internet]. 2020 Jul 25;396(10246):239–54. Available from: http://www.sciencedirect.com/science/article/pii/S0140673620310655
Landovitz RJ, Donnell D, Clement ME, Hanscom B, Cottle L, Coelho L, et al. Cabotegravir for HIV Prevention in Cisgender Men and Transgender Women. N Engl J Med. 2021/08/12 ed. 2021 Aug 12;385(7):595–608.
Kelley CF, Acevedo-Quiñones M, Agwu AL, Avihingsanon A, Benson P, Blumenthal J, et al. Twice-Yearly Lenacapavir for HIV Prevention in Men and Gender-Diverse Persons. N Engl J Med. 2024 Nov 27;
Nel A, van Niekerk N, Kapiga S, Bekker LG, Gama C, Gill K, et al. Safety and Efficacy of a Dapivirine Vaginal Ring for HIV Prevention in Women. N Engl J Med. 2016 Dec 1;375(22):2133–43.
Baeten JM, Palanee-Phillips T, Brown ER, Schwartz K, Soto-Torres LE, Govender V, et al. Use of a Vaginal Ring Containing Dapivirine for HIV-1 Prevention in Women. N Engl J Med. 2016 Dec 1;375(22):2121–32.
Molina JM, Ghosn J, Assoumou L, Delaugerre C, Algarte-Genin M, Pialoux G, et al. Daily and on-demand HIV pre-exposure prophylaxis with emtricitabine and tenofovir disoproxil (ANRS PREVENIR): a prospective observational cohort study. Lancet HIV. 2022/07/01 ed. 2022 Aug;9(8):e554–62.
Kibengo FM, Ruzagira E, Katende D, Bwanika AN, Bahemuka U, Haberer JE, et al. Safety, adherence and acceptability of intermittent tenofovir/emtricitabine as HIV pre-exposure prophylaxis (PrEP) among HIV-uninfected Ugandan volunteers living in HIV-serodiscordant relationships: a randomized, clinical trial. PLoS One. 2013/10/03 ed. 2013;8(9):e74314.
Herrera C, Serwanga J, Else L, Limakatso L, Opoka D, Ssemata AS, et al. Dose finding study for on-demand HIV pre-exposure prophylaxis for insertive sex in sub-Saharan Africa: results from the CHAPS open label randomised controlled trial. EBioMedicine. 2023 Jul;93:104648.
Traeger MW, Cornelisse VJ, Asselin J, Price B, Roth NJ, Willcox J, et al. Association of HIV Preexposure Prophylaxis With Incidence of Sexually Transmitted Infections Among Individuals at High Risk of HIV Infection. JAMA. 2019 Apr 9;321(14):1380–90.
Jenness SM, Weiss KM, Goodreau SM, Gift T, Chesson H, Hoover KW, et al. Incidence of Gonorrhea and Chlamydia Following Human Immunodeficiency Virus Preexposure Prophylaxis Among Men Who Have Sex With Men: A Modeling Study. Clinical Infectious Diseases [Internet]. 2017;65(5):712–8.
Hovaguimian F, Kouyos RD, Kusejko K, Schmidt AJ, Tarr PE, Bernasconi E, et al. Incidence of sexually transmitted infections and association with behavioural factors: Time-to-event analysis of a large pre-exposure prophylaxis (PrEP) cohort. HIV Med. 2024 Jan;25(1):117–28.
Abara WE, Bernstein KT, Lewis FMT, Schillinger JA, Feemster K, Pathela P, et al. Effectiveness of a serogroup B outer membrane vesicle meningococcal vaccine against gonorrhoea: a retrospective observational study. Lancet Infect Dis. 2022/04/16 ed. 2022 Jul;22(7):1021–9.
Molina JM, Bercot B, Assoumou L, Rubenstein E, Algarte-Genin M, Pialoux G, et al. Doxycycline prophylaxis and meningococcal group B vaccine to prevent bacterial sexually transmitted infections in France (ANRS 174 DOXYVAC): a multicentre, open-label, randomised trial with a 2 × 2 factorial design. The Lancet Infectious Diseases [Internet]. 2024 Oct 1 [cited 2024 Nov 3];24(10):1093–104. Available from: https://www.thelancet.com/journals/laninf/article/PIIS1473-3099(24)00236-6/abstract
Molina JM, Charreau I, Chidiac C, Pialoux G, Cua E, Delaugerre C, et al. Post-exposure prophylaxis with doxycycline to prevent sexually transmitted infections in men who have sex with men: an open-label randomised substudy of the ANRS IPERGAY trial. Lancet Infect Dis. 2017/12/13 ed. 2018 Mar;18(3):308–17.
Bachmann LH, Barbee LA, Chan P, Reno H, Workowski KA, Hoover K, et al. CDC Clinical Guidelines on the Use of Doxycycline Postexposure Prophylaxis for Bacterial Sexually Transmitted Infection Prevention, United States, 2024. MMWR Recomm Rep. 2024 Jun 6;73(2):1–8.
Sankaran M, Glidden DV, Kohn RP, Nguyen TQ, Bacon O, Buchbinder SP, et al. Doxycycline Postexposure Prophylaxis and Sexually Transmitted Infection Trends. JAMA Intern Med. 2025 Jan 6;
Kong FYS, Kenyon C, Unemo M. Important considerations regarding the widespread use of doxycycline chemoprophylaxis against sexually transmitted infections. J Antimicrob Chemother [Internet]. 2023 May 2 [cited 2024 Sep 23];78(7):1561–8. Available from: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10577522/
Langelier C, Chu V, Glascock A, Donnell D, Grabow C, Brown C, et al. Doxycycline post-exposure prophylaxis for sexually transmitted infections impacts the gut antimicrobial resistome. Res Sq. 2024 Apr 17;rs.3.rs-4243341.
Glidden DV, Amico KR, Liu AY, Hosek SG, Anderson PL, Buchbinder SP, et al. Symptoms, Side Effects and Adherence in the iPrEx Open-Label Extension. Clin Infect Dis. 2016/01/23 ed. 2016 May 1;62(9):1172–7.
Fux CA, Simcock M, Wolbers M, Bucher HC, Hirschel B, Opravil M, et al. Tenofovir use is associated with a reduction in calculated glomerular filtration rates in the Swiss HIV Cohort Study. Antivir Ther. 2008/02/05 ed. 2007;12(8):1165–73.
Pilkington V, Hill A, Hughes S, Nwokolo N, Pozniak A. How safe is TDF/FTC as PrEP? A systematic review and meta-analysis of the risk of adverse events in 13 randomised trials of PrEP. Journal of virus eradication. 2018/12/06 ed. 2018 Oct 1;4(4):215–24.
Clutterbuck D, Brady M, Rodger A, et al. Driving progress towards PrEP equity: Key changes in the 2025 BASHH/BHIVA UK PrEP guidelines. HIV Med 2025:1125-1141
Spinner CD, Lang GF, Boesecke C, Jessen H, Schewe K. Summary of German-Austrian HIV PrEP guideline. HIV Med. 2019/05/30 ed. 2019 Jul;20(6):368–76.
Kovari H, Sabin CA, Ledergerber B, Ryom L, Reiss P, Law M, et al. Antiretroviral Drugs and Risk of Chronic Alanine Aminotransferase Elevation in Human Immunodeficiency Virus (HIV)-Monoinfected Persons: The Data Collection on Adverse Events of Anti-HIV Drugs Study. Open Forum Infect Dis. 2016/03/01 ed. 2016 Jan;3(1):ofw009.
Mandala J, Nanda K, Wang M, De Baetselier I, Deese J, Lombaard J, et al. Liver and renal safety of tenofovir disoproxil fumarate in combination with emtricitabine among African women in a pre-exposure prophylaxis trial. BMC Pharmacol Toxicol. 2014/12/30 ed. 2014 Dec 24;15:77.
Radcke S, Dillon JF, Murray AL. A systematic review of the prevalence of mildly abnormal liver function tests and associated health outcomes. Eur J Gastroenterol Hepatol. 2014/11/08 ed. 2015 Jan;27(1):1–7.
Newsome PN, Cramb R, Davison SM, Dillon JF, Foulerton M, Godfrey EM, et al. Guidelines on the management of abnormal liver blood tests. Gut. 2017/11/11 ed. 2018 Jan;67(1):6–19.
EASL Clinical Practice Guidelines on non-invasive tests for evaluation of liver disease severity and prognosis – 2021 update. J Hepatol. 2021/06/25 ed. 2021 Sep;75(3):659–89.
McComsey GA, Tebas P, Shane E, Yin MT, Overton ET, Huang JS, et al. Bone disease in HIV infection: a practical review and recommendations for HIV care providers. Clin Infect Dis. 2010/09/16 ed. 2010 Oct 15;51(8):937–46.
Kasonde M, Niska RW, Rose C, Henderson FL, Segolodi TM, Turner K, et al. Bone mineral density changes among HIV-uninfected young adults in a randomised trial of pre-exposure prophylaxis with tenofovir-emtricitabine or placebo in Botswana. PLoS One. 2014/03/15 ed. 2014;9(3):e90111.
Mulligan K, Glidden DV, Anderson PL, Liu A, McMahan V, Gonzales P, et al. Effects of Emtricitabine/Tenofovir on Bone Mineral Density in HIV-Negative Persons in a Randomized, Double-Blind, Placebo-Controlled Trial. Clin Infect Dis. 2015/04/25 ed. 2015 Aug 15;61(4):572–80.